1983年,研究人员首次在绵羊网织红细胞中发现了外泌体,Johnstone等人在追踪网织红细胞成熟过程中的转铁蛋白受体(transferrin receptor)时发现,外泌体的形成是成熟红细胞中转铁蛋白受体发生丢失的机制。为与其他类型的细胞外囊泡(extracellular vesicles, EVs)区别开来,这类囊泡被命名为“外泌体”。
外泌体(Exosomes)是一类由细胞分泌的纳米级(40-100nm)球形脂质双分子层囊泡,内部富含核酸、蛋白质、脂质、细胞因子、转录因子受体等多种生物活性物质,主要通过细胞膜或内体膜出芽而形成。
几乎所有类型的正常细胞均能产生外泌体,例如人脐静脉内皮细胞、间充质干细胞、T 细胞、B 细胞、巨噬细胞、树突状细胞、自然杀伤细胞等。此外,上述细胞产生的外泌体还广泛存在于生物体液中,如唾液、血浆、尿液、腹水、乳汁及胆汁等。肿瘤细胞也可分泌大量外泌体,其表面携带的特异性抗原能表征其供体细胞(即来源肿瘤细胞)的特性。
外泌体可在生理与病理过程中发挥作用,作为细胞间通信和物质交换的关键媒介,因此在人类健康和疾病中发挥着关键作用,涉及发育、免疫应答、组织稳态、肿瘤发生和神经退行性疾病等多个生物学过程,基于这些特性,外泌体目前已成为多种疾病模型中具有潜力的治疗工具。
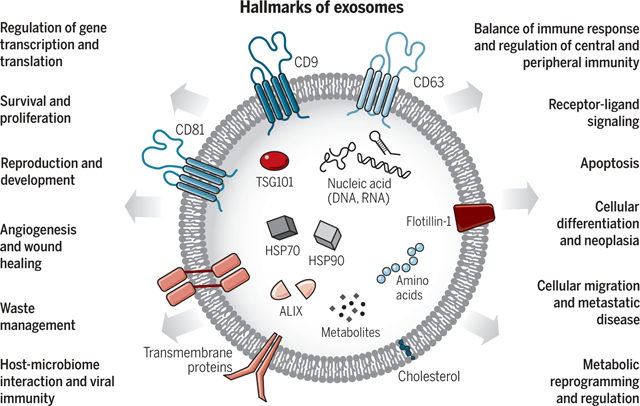
The structure of exosomes and their associated biological functions
(Science. 2020 Feb 7;367(6478):eaau6977)
外泌体表征及鉴定
鉴于外泌体来源广泛且功能重要,对其进行准确鉴定与表征便成为研究的关键。根据国际细胞外囊泡学会(International Society for Extracellular Vesicles, ISEV)在2014年提出的外泌体鉴定的3个标志:透射电镜(transmission electron microscope,TEM)、粒径(Nanoparticle Tracking Analysis, NTA)、蛋白标志物(Western Blot, WB),为了确认分离出的囊泡确实是外泌体,并排除其他细胞外囊泡(如微囊泡)的污染,需要对其进行严格的鉴定,图3为常用的外泌体表征手段。
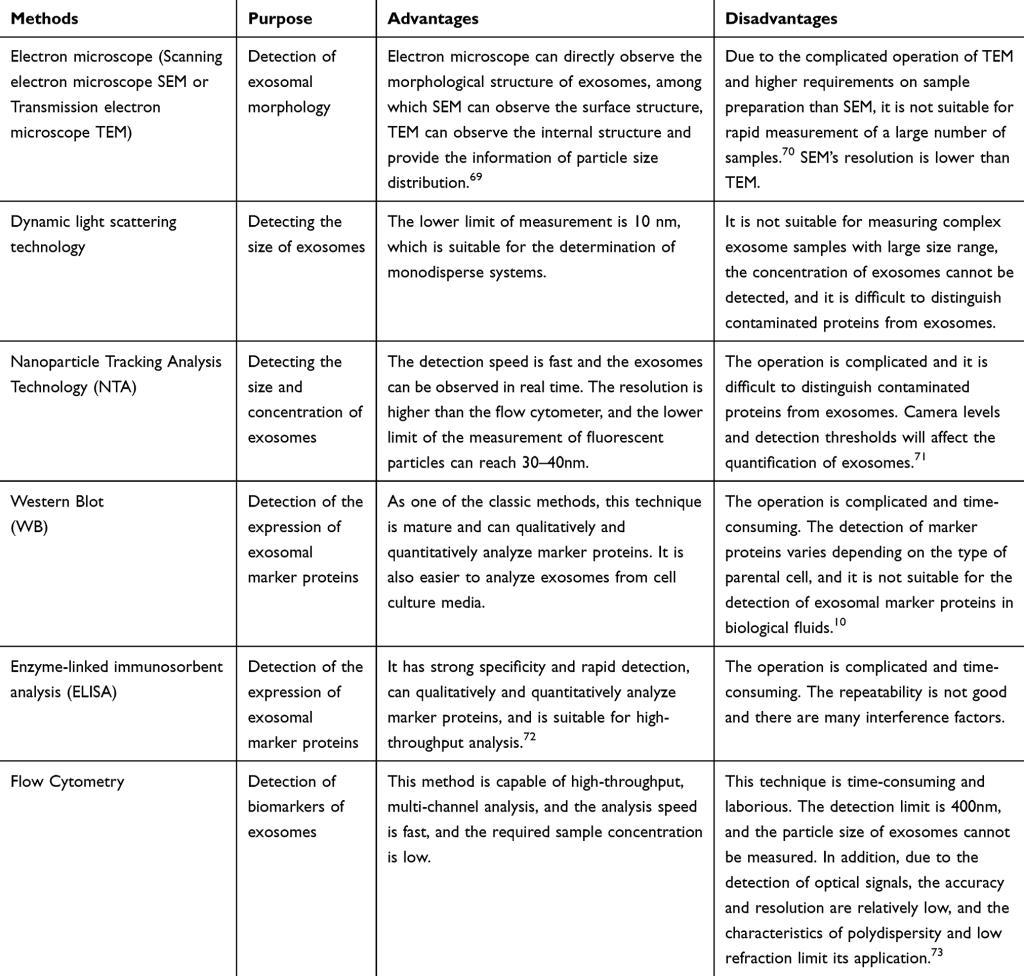
Purpose, Advantages and Disadvantages of Common Exosome Characterization Methods
(Int J Nanomedicine. 2020 Sep 22:15:6917-6934.)
外泌体标志物
所有外泌体都含有一些共同的蛋白质,例如参与运输机制的热休克蛋白84(Hsp84)、肿瘤易感基因101(TSG101)和Alix。内体ESCRT系统是形成多泡体(MVBs)所需膜内陷过程的一系列蛋白质复合物,由ESCRT-0、ESCRT-I、ESCRT-II、ESCRT-III和Vps4-Vta1五个蛋白复合体及若干相关蛋白组成。ESCRT复合物组分、GTP酶、Rab蛋白、四跨膜蛋白及其他蛋白质在外泌体的识别、摄取、释放和内化过程中发挥作用。
在外泌体鉴定中,通常会检测Alix、TSG101、Hsp70和CD9等外泌体标志物。其他常见的外泌体蛋白还包括:
四跨膜蛋白:CD9、CD81、CD82、tetraspanin-8;
热休克蛋白:Hsp84、HSP70、HSP90;
受体:CD46、CD55、NOTCH1;
膜黏附蛋白:如整合素;
膜运输/ trafficking相关蛋白:膜联蛋白、Rab蛋白家族;
细胞骨架成分:ezrin、actin、tubulin、cytokeratins、myosin;
溶酶体标志蛋白:溶酶体相关膜蛋白1/2、组织蛋白酶D、CD63;
抗原呈递蛋白:如HLA I类和II类/肽复合物;
代谢酶:GAPDH、丙酮酸激酶;
蛋白酶:ADAM10、DPEP1、ST14;
转运蛋白:ATP7A、ATP7B、MRP2、SLC1A4、SLC16A1、CLIC1。
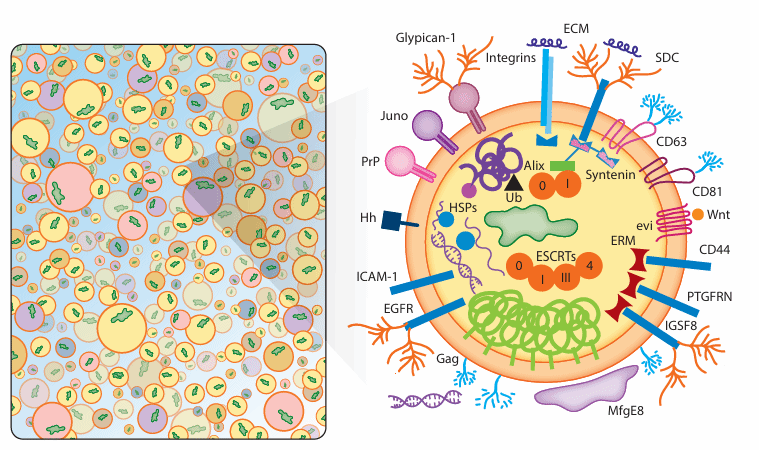
Exosome biomarkers
(Annu Rev Biochem. 2019 Jun 20:88:487-514)
AntibodySystem提供外泌体阳性及阴性标志物的高质量抗体产品,能够为外泌体与疾病相关的基础研究提供有力支持!
|
货号 |
产品名称 |
|
RHC69302 |
Anti-HSP70 Antibody (R1M49) |
|
RHE05802 |
Anti-HSPA4/HSP70 Antibody (R3J59) |
|
FHD48812 |
Anti-Human CD9 Antibody (SAA0003), PE |
|
RHD48802 |
Anti-Human CD9 Nanobody (SAA0905) |
|
DHD48801 |
Research Grade Anti-Human CD9 (AT14-012) |
|
VHD48801 |
InVivoMAb Anti-Human CD9 Antibody (Iv0274) |
|
RHC37602 |
Anti-CD63 Antibody (R3B43) |
|
RMC37601 |
Anti-CD63 Antibody (R1L87) |
|
FHF34010 |
Anti-Human CD81 Antibody (5A6) |
|
RHF34002 |
Anti-CD81 Antibody (R1Z70) |
|
RHJ47103 |
Anti-TSG101 Antibody (R3W11) |
|
VHJ47102 |
InVivoMAb Anti-Human TSG101 Antibody (Iv0254) |
|
RHJ47102 |
Anti-TSG101 Antibody (R2J91) |
|
PHJ29601 |
Anti-PDCD6IP Polyclonal Antibody |
|
RHJ29604 |
Anti-PDCD6IP/ALIX Antibody (R2J32) |
|
RHJ29603 |
Anti-PDCD6IP Antibody (R2J31) |
|
PHG16101 |
Anti-GM130/GOLGA2 Polyclonal Antibody |
|
RHG16103 |
Anti-GM130/GOLGA2 Antibody (R3R68) |
|
RHB37201 |
Anti-FLOT1 Antibody (R1B06) |
|
RMB37201 |
Anti-FLOT1 Antibody (R2V99) |
|
RHE80601 |
Anti-RAB27A Antibody (R3M45) |
|
RHF37503 |
Anti-ACTB/β-actin/Beta Actin Antibody (R3N80) |
|
RHC09001 |
Anti-GAPDH Antibody (R2Y76) |
参考文献
1. Rezaie J, Feghhi M, Etemadi T. A review on exosomes application in clinical trials: perspective, questions, and challenges. Cell Communication and Signaling. 2022;20(1).
2. Xu G, Jin J, Fu Z, et al. Extracellular vesicle-based drug overview: research landscape, quality control and nonclinical evaluation strategies. Signal Transduction and Targeted Therapy. 2025;10(1).
3. Kurian TK, Banik S, Gopal D, Chakrabarti S, Mazumder N. Elucidating Methods for Isolation and Quantification of Exosomes: A Review. Molecular Biotechnology. 2021;63(4):249-266.
4. Pegtel DM, Gould SJ. Exosomes. Annual Review of Biochemistry. 2019;88(1):487-514.
5. Zhang Y, Bi J, Huang J, Tang Y, Du S, Li P. Exosome: A Review of Its Classification, Isolation Techniques, Storage, Diagnostic and Targeted Therapy Applications. International Journal of Nanomedicine. 2020;15:6917-6934.